2026年4月16日、潰瘍性大腸炎の治療を続けていらっしゃる方にとって、ちょっと嬉しいニュースが発表されました。
「オンボー皮下注200mg製剤」が、潰瘍性大腸炎の維持療法に使えるようになりました。
「新薬が出たの?」と思われた方もいらっしゃるかもしれません。でも実は、オンボー(一般名:ミリキズマブ)というお薬そのものは、2023年から既に潰瘍性大腸炎の治療で使われてきたものです。
では、何が変わったのか? 一言でいえば——
4週ごとの注射が「2本」から「1本」に減る
「それだけ?」と思うかもしれません。でも、維持療法を何年も続けていらっしゃる患者さんにとって、これは決して小さな変化ではないのです。
消化器内科医として炎症性腸疾患(IBD)の診療に携わる立場から、今回の承認の意味を、できるだけやさしい言葉でお伝えします。
そもそもオンボーってどんな薬?
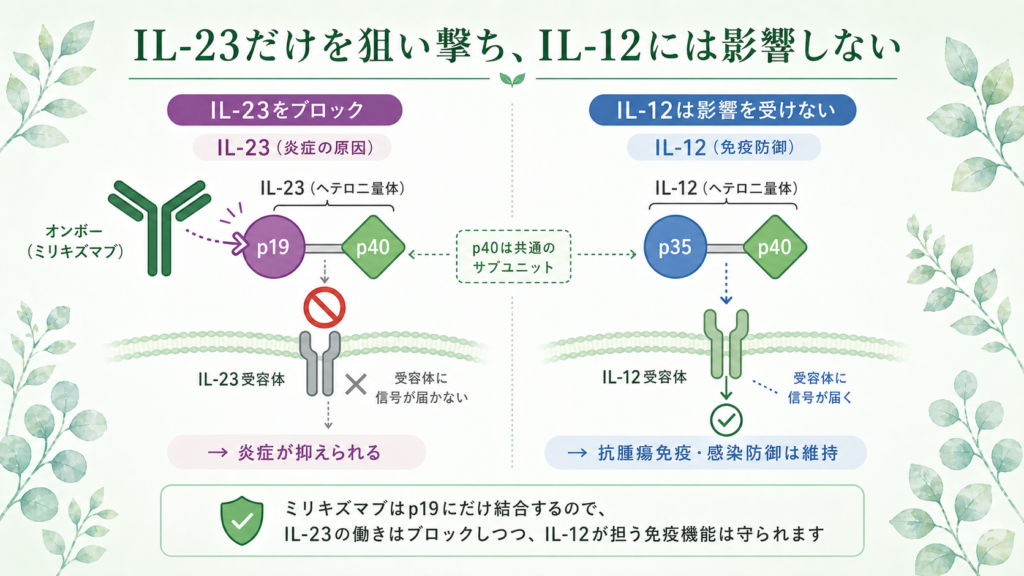
オンボー(ミリキズマブ)は、「生物学的製剤」と呼ばれるタイプのお薬です。
潰瘍性大腸炎の腸の炎症を引き起こす犯人の一つに、「IL-23(インターロイキン23)」という体の中の物質があります。オンボーは、このIL-23の中の「p19」という部分だけを狙い撃ちしてブロックすることで、炎症を抑える仕組みです。
ポイントをまとめると、
- 2023年3月27日に日本で製造販売承認、同年6月に発売
- 同じクラスの薬では世界で初めて潰瘍性大腸炎治療薬として承認された
- 「5-ASA製剤やステロイド、他の生物学的製剤でも症状が残ってしまう」中等症から重症の方が対象
- 最初に点滴で強力に炎症を抑える(寛解導入)→ その後、皮下注射で状態を保つ(維持療法)という2段階で使う
維持療法は、症状が落ち着いた状態を長く保つための、いわば「長距離走」のような治療です。潰瘍性大腸炎は慢性の病気ですから、多くの方が何年、何十年と付き合っていくことになります。
これまでの維持療法 ― 実は「毎回2本打っていた」
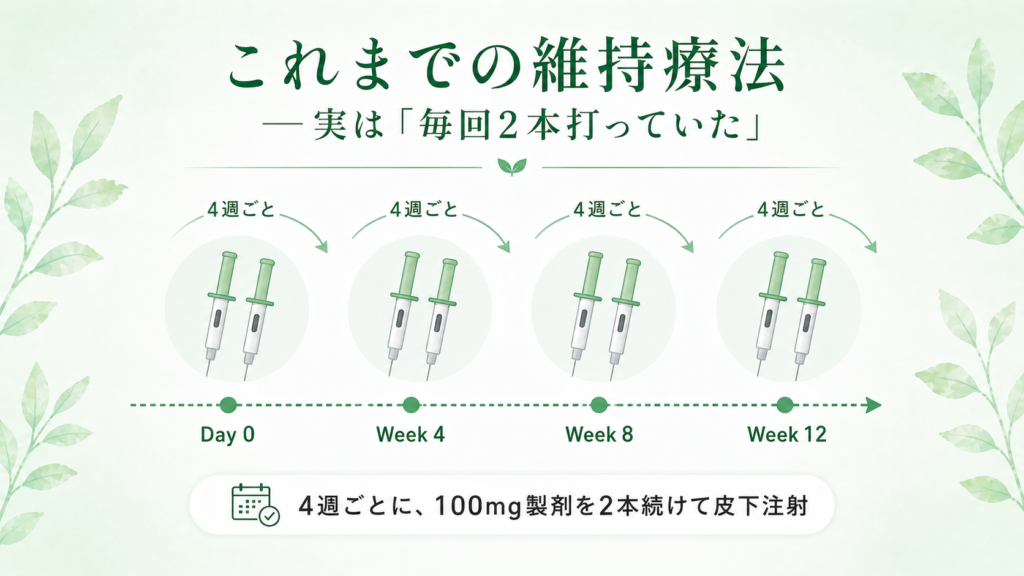
ここが今回の話の核心です。
これまでオンボーで維持療法を受けていた患者さんは、4週に1回、クリニックや病院で100mg製剤を「2本」続けて注射されていました。なぜ2本かというと、維持療法に必要な量が200mgなのに対して、これまで使える皮下注射の製剤は100mg製剤しかなかったからです(200mg製剤は、それまでクローン病治療にのみ承認されていました)。
患者さんからすると、診察室のベッドに横になって、1本目を打ち、少し針を刺す場所を変えて2本目を打つ——この流れを、4週ごとに続けていたわけです。
2026年4月16日、何が変わったのか
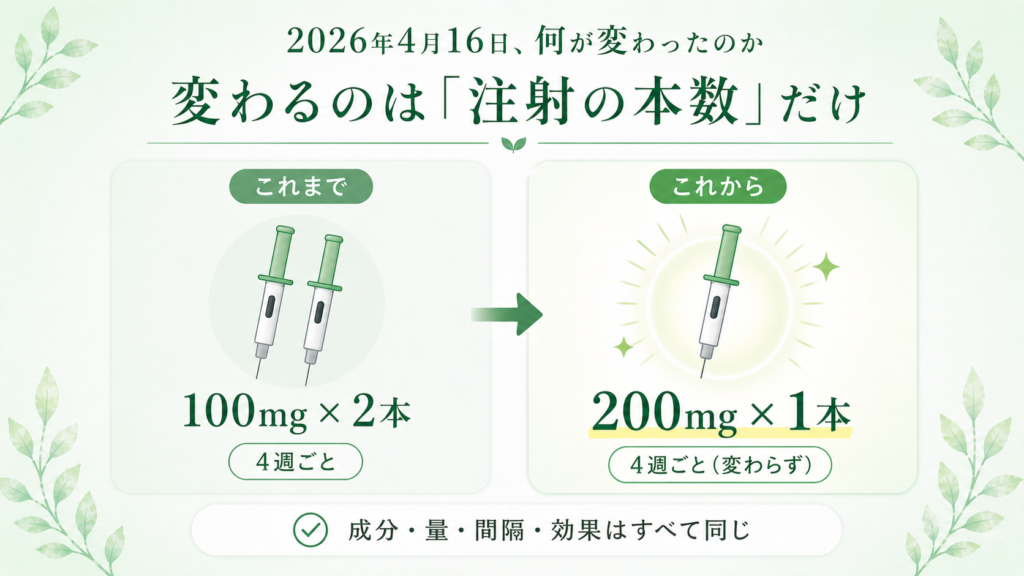
今回承認されたのは、オンボー皮下注「200mg」製剤の、潰瘍性大腸炎維持療法への適応追加です。
これまで200mg製剤は「クローン病のみ」に使える製剤でしたが、今回の承認により、潰瘍性大腸炎の維持療法でも使えるようになりました。
| 項目 | これまで | これから |
|---|---|---|
| 1回の注射本数 | 100mg × 2本 | 200mg × 1本 |
| 投与間隔 | 4週に1回 | 4週に1回(変わらず) |
| 投与量 | 200mg | 200mg(変わらず) |
| 製剤の形 | オートインジェクター / シリンジ | オートインジェクター / シリンジ(変わらず) |
つまり、お薬の成分も、量も、間隔も、効き方も変わりません。変わるのは「注射の本数」だけ。でも、それが維持療法を続ける患者さんにとっては、とても意味のある変化なのです。
注射が「1本」になることの、ささやかだけど確かな意味
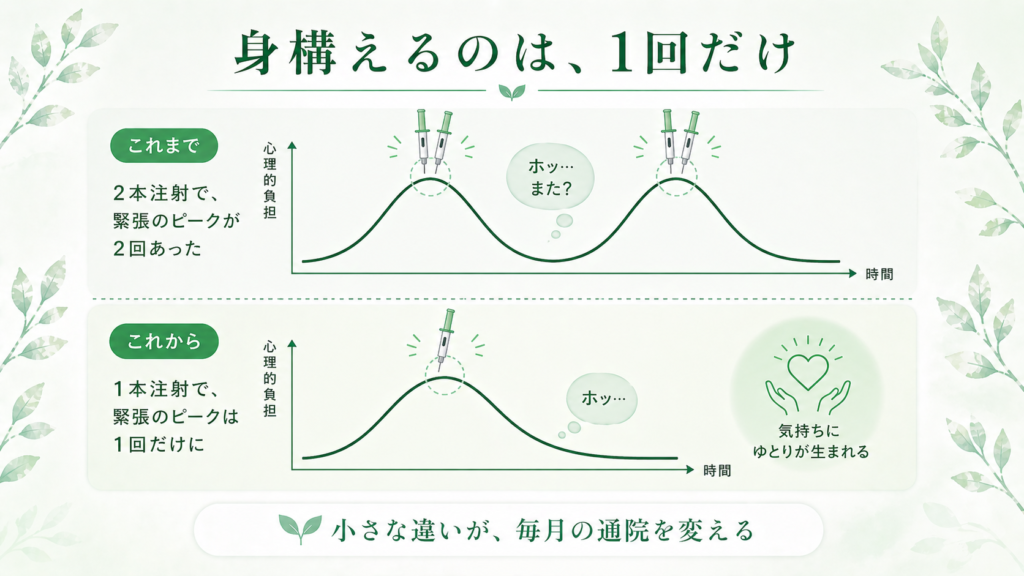
ここからは、医師として日々の臨床で感じている一般的な観察を交えてお話しします。
維持療法を長く続けていらっしゃる患者さんと話していると、「注射の回数」そのものよりも、「身構えることが2回ある」という心理的な重さを負担に感じている方が多いことに気づきます。1本目が終わってホッとしたと思ったら、もう1本ある——この切り替えが、案外しんどいのです。
「1本で済む」ということは、この心理的な切り替えが半分で終わるということ。刺す部位も1か所で済むので、注射部位の違和感や皮膚反応が出る可能性も物理的には減ります。
上記の「負担が軽くなる」という点は、製剤設計上の論理的な利点であって、「患者さんの満足度がこれだけ改善した」といった数値で示されたデータを私は確認できていません。あくまで「2本から1本に減ることで、理屈としては楽になるはず」という範囲のお話とご理解ください。
それでも、維持療法は1回きりの治療ではなく、何年も、場合によっては一生続けていく治療です。1回あたりのわずかな負担の違いも、積み重なれば生活の質に影響します。
お薬そのものの効果は、これまでと同じ

ここも患者さんに正しく知っていただきたいポイントです。
オンボーの有効性や安全性は、今回の承認で「新たに証明された」わけではありません。もともと有効性が確認されていたお薬について、「投与するための容器の選択肢が増えた」という位置づけです。
オンボーは、2つの国際共同第3相試験によってその効果が示されています。
- LUCENT-1試験(12週間の寛解導入試験)
- LUCENT-2試験(40週間の維持試験)
これらの試験では、他の生物学的製剤やJAK阻害薬でも十分な効果が得られなかった患者さんも含めて、プラセボに比べて有意な改善が確認されています。便意切迫感(突然のトイレへの強い衝動)についても改善効果が報告されています。
維持療法を受けている方は、「薬そのものが変わる」という不安を感じる必要はありません。同じお薬を、同じ量、同じ間隔で、ただ「1本の注射で」受けられるようになる——そう理解していただくのが正確です。
気になる「切り替え」について
すでに100mg製剤を2本で維持療法を受けていらっしゃる方が、自動的に200mg製剤1本に切り替わるわけではありません。切り替えのタイミングや判断は、主治医の先生と相談することになります。
また、切り替えにあたっては以下の点を確認しておかれるとよいと思います。
- 薬価(費用):200mg製剤の薬価収載情報は、本記事執筆時点(2026年4月24日)で私は最新情報を確認できていません。費用面は主治医や薬剤師にご確認ください
- 発売時期:承認 = すぐ使えるではありません。実際に医療機関で使えるようになるまでには、薬価収載などのステップがあります
- 100mg製剤と200mg製剤の生物学的同等性:電子添文には「100mg製剤と200mg製剤の生物学的同等性は示されていない」という記載があります(※これはクローン病での投与量調整に関する注意書きで、UC維持療法で規定量の200mgを投与する限り問題になるものではありませんが、念のため主治医にご確認ください)
「症状がないうちに腸を守る」ために

潰瘍性大腸炎の維持療法は、「症状が落ち着いた今こそ、続けることが大事」な治療です。調子が良いと「もう薬、やめてもいいのでは?」と思いがちですが、自己判断での中断は再燃(症状の再発)の大きなリスクになります。
今回のような、「治療の本質は変わらないけれど、続けやすさが少し改善される」というニュースは、派手ではありませんが、患者さんの日常に地続きで届く大切な進歩だと思います。
診察の際に、「今回の話題、先生どう思う?」と主治医の先生に一言聞いてみていただくのも良いかもしれません。治療選択肢が増えたことを知っておくだけで、これからの通院が少し違って感じられるはずです。
参考にした主な情報源
- Medical Tribune 新薬エクスプレス「オンボー、潰瘍性大腸炎の維持療法に対し適応追加承認を取得」(2026年4月16日)
https://medical-tribune.co.jp/rensai/articles/?blogid=11&entryid=571631(医師限定の一部含む) - ミクスOnline「日本イーライリリーと持田製薬 オンボー200mg皮下注製剤 UC維持療法の適応追加の承認取得」
https://www.mixonline.jp/tabid55.html?artid=80091 - 持田製薬 適時開示(2026年4月16日):日経会社情報DIGITAL経由
https://www.nikkei.com/nkd/disclosure/tdnr/20260416505152/ - KEGG 医療用医薬品情報:オンボー皮下注100mgオートインジェクター 他(電子添文)
https://www.kegg.jp/medicus-bin/japic_med?japic_code=00071661 - 日経メディカル「IL-23p19を標的とする潰瘍性大腸炎治療薬」(2023年)
https://medical.nikkeibp.co.jp/leaf/all/series/drug/update/202306/579987.html
※本記事は2026年4月24日時点の情報に基づきます。薬剤の使用にあたっては、必ず主治医・薬剤師にご相談ください。記事内のリンク先は公開時点で有効性を確認していますが、各サイト側の都合で変更・削除される可能性があります。





コメント