*このサイトはアフィリエイト広告(Amazonアソシエイト含む)を掲載しています。
背景・目的
日本人の潰瘍性大腸炎患者を対象に、1日1回投与の経口ヤヌスキナーゼ1優先阻害薬であるfilgotinibの安全性と有効性を、第2b/3相SELECTION試験で検討した。
方法
SELECTION試験(NCT02914522)は、2つの導入試験と1つの維持試験からなる無作為化プラセボ対照試験である。中等度から重度の活動性のUC患者を、導入試験A(生物学的製剤未使用)またはB(生物学的製剤経験者)に無作為に割り付け、フィルゴチニブ200mg、100mg、またはプラセボを1日1回、11週間投与した。10週目に臨床的寛解またはMayo Clinic scoreによる奏効が得られた患者は、47週間の維持療法試験に参加した。有効性と安全性の結果は、日本で登録された日本人患者を対象に評価された。
結果
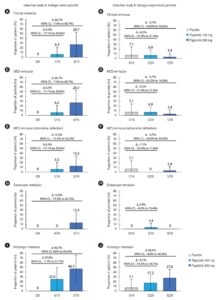
日本では、導入試験Aで37例、導入試験Bで72例の日本人が登録され、54例が維持試験に登録された。導入試験A(4/15例[26.7%]、0/6例[0%])および維持試験(5/20例[25.0%]、0/9例[0%])では、フィルゴチニブ200 mg投与群がプラセボ投与群より高い割合で臨床的寛解を達成したが、導入試験B(1/29例[3.4%]、1/14例[7.1%])ではこれは認められなかった。いずれの用量も忍容性は良好であり、新たな安全性シグナルは認められなかった。なお、導入試験A(2.3%、1/44)および維持試験(5.0%、1/20)において、フィルゴチニブ200 mg投与患者1名に帯状疱疹が報告された。

結論
これらのデータは、SELECTION試験全体のデータと同様に、日本人UC患者に対するフィルゴチニブ200mgの有効な治療選択肢となる可能性を示唆するものである。ただし、患者数が少ないため、データの解釈には慎重を期す必要がある。
感想
寛解導入率はBioナイーブの患者ではまあまあですが、Bio経験者はかなり残念な結果となってしまいました。論文中ではnが少ないためデータの解釈には慎重を期す必要があると記載されていますが、nはフィルゴチニブ100mg, 200mgのグループはそれぞれ30例弱とほどほどあります。この結果を見るとBio経験者に対する導入期でのフィルゴチニブの寛解導入率は低いと言わざるを得ないと思います。
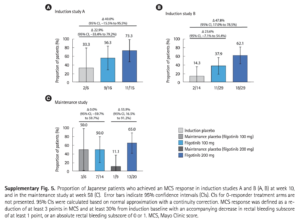
しかしながらSupplementary Fig.5で示されているように、導入期でのフィルゴチニブ200mg投与群のMCS(Mayo Clinic score) responseは、Bioナイーブで73%, Bio経験者でも62%と高い反応性を示しています。すなわちBio経験者には導入期での寛解導入は期待できないが、症状改善は期待できる薬剤と考えられます。
論文
Hibi T, et al: Efficacy and safety of filgotinib as induction and maintenance therapy for Japanese patients with moderately to severely active ulcerative colitis: a post-hoc analysis of the phase 2b/3 SELECTION trial. Intest Res. 2022 Mar 11. doi: 10.5217/ir.2021.00143. Online ahead of print.
最後までお読みいただきありがとうございました!





コメント