*このサイトはアフィリエイト広告(Amazonアソシエイト含む)を掲載しています。
背景
パクリタキセルまたはナノ粒子アルブミン結合パクリタキセルとラムシルマブの併用療法(PTX/nab-PTX + RAM)は、進行胃癌(AGC)の二次化学療法として広く用いられているが、このレジメンではしばしば重症の好中球減少が発生する。これまでの研究で、重症の好中球減少はがん化学療法における予後良好因子であることが報告されているが、PTX/nab-PTX+RAMを投与されているAGC患者においては不明な点がある。また、早期重症好中球減少症(EOSN)の危険因子もいまだ不明である。
方法
2017年1月から2020年6月までに2次治療として4週ごとにPTX/nab-PTX(第1、8、15日目)+RAM(第1、15日目)の治療を受けたAGC患者のうち、治療前にグレード0または1の好中球減少が見られた患者について、レトロスペクティブに検討した。
血液検査は毎回治療当日に行い、病勢進行は主に8±2週間ごとにCTで判定した。
EOSNは、最初の28日間に発生したグレード4の好中球減少症と定義された。EOSNの危険因子は、多変量ロジスティック回帰分析を用いて検討した。EOSNの有無による無増悪生存期間(PFS)と全生存期間(OS)をCox比例ハザードモデルによる多変量解析で検討した。
結果
244名の患者の臨床データを解析した。EOSNは51例(20.9%)に認められた。
多変量解析により、EOSNの危険因子として、65歳以上(オッズ比2.75)、原発巣の存在(同2.82)、腹膜転移の存在(同2.52)、グレード1の好中球減少(同3.32)、ALP高値(同2.34)の5つが同定された。
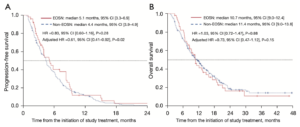
PFSはEOSNを有する患者においてEOSNを有さない患者よりも有意に長く[調整後ハザード比(HR)、0.61;95%CI、0.41-0.92]、OSはEOSNを有する患者においてEOSNを有さない患者よりも長い傾向があった(調整後HR、0.73;95%CI、0.47-1.12)。HRは、予測因子または予後因子として重要と考えられる患者背景因子および血液検査データで調整された。
結論
EOSNは、PTX/nab-PTX+RAMによる治療を受けたAGC患者の良好な転帰と関連する可能性がある。危険因子を考慮した上で慎重に治療を行う必要がある。
感想
PTX/nab-PTX+RAMの治療を受けた患者ではEOSNを発症した方がPFSが良いこと、またEOSNのrisk factorについて検討した論文です。
ただし実臨床ではGrade4の好中球減少が起きた場合には、FN一歩手前であるためかなりヒヤヒヤします。FNを発症していなくても、発症した際に重篤になるリスクが高い人は入院が必要になるかもしれません。臨床医としては患者の安全のためにできればGrade4の好中球減少を起こさないように化学療法の容量調節を行っていきたいものです。
またEOSNの患者ではPFSは延長しましたが、OSは延長しませんでした。このようにPFSが改善してもOSが改善するとは限らないことが実臨床の難しさです。
出典
Hagiwara Y, et al; Risk factors and efficacy outcomes of early-onset severe neutropenia due to paclitaxel or nanoparticle albumin-bound paclitaxel combined with ramucirumab in advanced gastric cancer: a multicenter retrospective cohort study. J Gastrointest Oncol. 2022 Dec;13(6):2769-2778. doi: 10.21037/jgo-22-499.
最後までお読みいただきありがとうございました!


コメント